Проведены квантово-химические расчеты с помощью программы МОРАС-2009 структурных, энергетических и электронных характеристик молекул химических добавок-пластификаторов с различными функциональными группами и энергии образования комплексов с гидратированным трехкальциевым силикатом.
Quantum-chemical calculations using MOPAC-2009 structural, energetic and electronic characteristics of molecules of chemical additives plasticizers with different functional groups and the energy of formation of complexes with hydrated tricalcium silicate.
ВВЕДЕНИЕ
Проблема выявления взаимосвязи между строением (структурой) органического соединения и проявляемыми им свойствами, например, между электронным строением и пластифицирующей способностью, строением и сорбцией к минералам цементного клинкера, степенью замедления твердения и т. д. является актуальной задачей практической органической химии добавок-пластификаторов для цементного бетона, так как ее решение для отдельных классов или групп соединений повышает эффективность эксперимента по созданию новых пластификаторов с заданными свойствами.
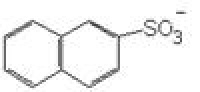
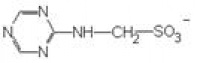
Как показано в работах [1–4], эффективность влияния органических соединений на свойства цементных композиций определяется природой активных групп. Пластифицирующий эффект при введении в минеральные вяжущие органических соединений нужно ожидать при сочетании следующих факторов: наличия большого углеводородного радикала и функциональных групп, способных реагировать с минералами вяжущего или продуктами его гидратации. Функциональные группы в свою очередь могут обладать электронодонорными (анионы или молекулы, содержащие атомы с неподеленными электронными парами: НО?, RO?, Cl?, RCOO?, CN?, R?, NH2?, H2O, NH3?, C2H5OH и др.) или электроноакцепторными свойствами (катионы: H+?, Cl?, NO-2?, SO3H?, R?, R?C=O). Соответственно заместители первой группы способны отдавать электронную пару для образования новой связи, а второй группы – используют чужую пару электронов и создают донорно-акцепторные комплексы с минералами цемента и продуктами его гидратации. При этом однозарядные ионогенные группы оказывают меньшее влияние на пластификацию и твердение по сравнению с многозарядными группами.
Влияние функциональной группы на твердение цементного геля усиливается, если в пара-положении к одной группе находится другая полярная группа, а также с увеличением гибкости основной цепи молекулы добавки-пластификатора. Наличие двойных связей, бензольного или нафталинового кольца повышает жесткость структуры молекулы и уменьшает ее отрицательное влияние на структурообразование цементного геля.
Поэтому изменением вида и количества функциональных групп в молекуле добавки (при смешивании нескольких компонентов или специальной обработкой) изменяют энергию взаимодействия добавок с гидратированными частицами цемента и, соответственно, особенности влияния ее на свойства цементных композиций. Такой подход успешно реализован при химической модификации лигносульфонатов [5], что позволило приблизить их по эксплуатационным характеристикам к суперпластификатору С-3, а также при разработке гиперпластификаторов [6], основой которых явились сополимеры производных акриловых кислот с различными функциональными группами в своем составе.
В статье показано определение структурных и энергетических характеристик добавок-пластификаторов в зависимости от вида функциональной группы, а также приведены расчеты энергии образования комплекса с гидросиликатом кальция.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Авторами статьи проведены квантово-химические расчеты структурных, энергетических и электронных характеристик молекул химических добавок-пластификаторов с различными функциональными группами и энергии образования комплексов с гидратированным трехкальциевым силикатом. Расчеты выполнены с помощью программы МОРАС-2009 с использованием полуэмпирического Гамильтонианина РМ6 [7, 8]. Энергию образования комплекса определяли по разности между теплотой образования комплекса АВ и теплотой образования простых веществ А и В по формулам:
![]() (1)
(1)
![]() (2)
(2)
Результаты расчетов приведены в таблице 1. Добавки содержат ионогенные и неионогенные группы. Поскольку полуэмпирические приближения не в полной мере описывают структуру гидратов ионов металлов, в модельной системе катионы (Na+) непосредственно взаимодействуют с тоберморитом (с обратной стороны слоя). Энергия взаимодействия катиона с тоберморитом является постоянной для всех рассматриваемых вариантов взаимодействия добавок. В свою очередь величина энергии образования комплекса несколько завышена на разницу между энергиями взаимодействия гидратированного и негидратированного катиона с тоберморитом. Энергетический эффект отражает взаимодействие единичной молекулы добавки с поверхностью кристаллогидратов С3S и характеризует прочность образуемого комплекса. Итоговая величина энергии взаимодействия зависит от степени заполнения адсорбционного слоя, степени дефектности поверхности кристалла и других факторов.
Таблица 1. Расчетные параметры функциональных групп химических добавок
Энергия химической связи равна работе, которую необходимо затратить, чтобы разделить молекулу на две части (атомы, группы атомов) и удалить их друг от друга на бесконечное расстояние. В зависимости от частиц, образующих химическую связь, характера взаимодействия между ними (вида связи), кратности связи (одинарные, двойные и тройные связи) энергия связи составляет: для ковалентной связи – от 100 до 1000 кДж/моль, для ионной связи – от 100 до 20 000 кДж/моль, для водородных связей – 10–50 кДж/моль, для Ван-дер-Ваальсовых взаимодействий – 0,1–1,0 кДж/моль [9]. Связь считается прочной, или сильной, если ее энергия превышает 500 кДж/моль, слабой – если ее энергия менее 100 кДж/моль. Если при взаимодействии атомов выделяется энергия менее 15 кДж/моль, то считается, что химическая связь не образуется, а имеет место межмолекулярное взаимодействие. Таким образом, энергия химической связи – важная характеристика, определяющая реакционную способность вещества. Применительно к взаимодействию химических добавок с гидратами минералов цемента она характеризует устойчивость образующихся комплексов, конкурентоспособность химических добавок к взаимодействию по сравнению с молекулами воды.
Как видно из таблицы 1, энергии взаимодействия функциональных групп химических добавок с гидратированным C3S значительно различаются: от 38 до 527 кДж/моль. Наименьшей энергией связи обладают аминогруппы – 38,46 кДж/моль, что гораздо меньше, чем у молекул воды – 54,52 кДж/моль. Сравнимой энергией связи с молекулами воды обладают фенольные (50,19 кДж/моль) и спиртовые ОН-группы – 54,18 кДж/моль. Расчеты показывают, а опыты подтверждают, что добавки, содержащие такие группы (например, упаренная последрожжевая барда), обладают слабым пластифицирующим действием на цементный гель. Наибольшую энергию связи имеют карбоксильные группы – 527,85 кДж/моль, немного меньшую – нитрогруппы – 474,73 кДж/моль и сульфогруппы – 416,20 кДж/моль. С увеличением энергии связи молекулы добавки-пластификатора более конкурентоспособны по сравнению с водой, адсорбируются на гидролизованной поверхности цементных частиц и часть воды выталкивают с ее поверхности, что способствует пластификации.
Следует отметить, что химическая природа остатка, связанного с функциональной группой, незначительно влияет на энергию образования комплекса. Например, для сульфогруппы энергия связи составляет в алкиларилсульфонатах 407,16 кДж/моль, а в алкилнафталинсульфонатах 414,86 кДж/моль. Природа остатка с функциональной группой и конформационная структура молекулы добавки определяют характер образования адсорбционных слоев и, соответственно, степень замедления гидратации цементного вяжущего. Молекулы нитроната эпихлоргидрина обладают большой энергией комплексообразования (579,57 кДж/моль, содержат три функциональные группы) и, как следствие, при введении в сравнимых количествах существенно замедляют твердение цементного геля.
Таким образом, способ изменения вида и количества функциональных групп добавки, конформации молекулы, длины привитых цепей позволяет управлять пластифицирующей способностью добавки, изменять стойкость получаемых комплексов и успешно применяется в процессе модификации существующих известных добавок [5] и при разработке новых [1, 6, 10].
Как было показано ранее [3], в зависимости от вида и количества функциональных групп в молекуле добавки, ее молекулярной массы, наличия привитых боковых цепей в процессе пластификации цементной композиции может преобладать электростатический эффект за счет выталкивания молекул воды из адсорбционного слоя в диффузный (обычные пластификаторы и суперпластификаторы) или стерический эффект действия добавки в диффузном слое (суперпластификаторы и гиперпластификаторы). Степень влияния добавок на протекание реакций гидратации определяется особенностями строения органоминеральной адсорбционной пленки, обусловленными различным пространственным расположением макромолекул в адсорбционной пленке (определяется конформационной структурой молекулы), видом и положением функциональных групп и различиями в энергии связи их с гидратированными частицами цемента.
С учетом ранее проведенных исследований по величине дипольного момента добавок-пластификаторов и его взаимосвязи с величиной водоредуцирующей способности [11], предлагается система (таблица 2) критериальной оценки эффективности добавок-пластификаторов по следующим показателям:
– энергия образования комплексов ?Hf, кДж/моль;
– дипольный момент молекулы D;
– концентрационная активность добавки Ка, определяемая по формуле
![]() (3)
(3)
где ?Пmin, ?Пmax – соответственно увеличение подвижности смеси (см) от исходной при минимальном Dmin и максимальном Dmax количестве добавки (%).
Концентрационная активность добавки Ка характеризуется тангенсом угла наклона кривой изменения подвижности смеси с увеличением количества добавки.
Как видно из таблицы 2, добавки III–IV групп, или слабопластифицирующие, обладают энергией образования комплексов и дипольным моментом, сравнимыми с молекулами воды, и характеризуются наибольшим значением концентрационной активности Ка.
Таблица 2. Критерии оценки добавок-пластификаторов
| Группа эффективности | Критерии оценки | |||
|---|---|---|---|---|
| По СТБ 1112 [12] | По ГОСТ 24211-2008 | Энергия образования комплекса ?Hf, кДж/моль | Дипольный момент молекулы D | Концентрационная активность Ка |
| I | I | Более 400 | Более 4,0 | Не более 15 |
| II | II | 200–350 | 2,5–4,0 | 15–30 |
| III–IV | Менее 100 | Менее 2,2 | Более 30 | |
ЗАКЛЮЧЕНИЕ
Разработка пластифицирующих добавок не самоцель, а возможность решения конкретных задач технологии бетонов: повышение подвижности смесей, морозо- и коррозионной стойкости; получение самоуплотняющихся, высокопрочных и быстротвердеющих бетонов и т. д. Поэтому установление взаимосвязи между структурой добавок и их свойствами позволяет вести целенаправленный поиск новых добавок, расширять их номенклатуру применительно к задачам технологии бетонов.
СПИСОК ЛИТЕРАТУРЫ
1. Батраков, В. Г. Модифицированные бетоны. Теория и практика, 2-е изд. / В. Г. Батраков. – М.: Стройиздат, 1998. – 768 с.
2. Рахимбаев, Ш. М. Исследование закономерностей влияния состава вяжущих и добавок на основные свойства тампонажных материалов: автореф. дис. … д-ра техн. наук: 05.23.05 / Ш. М. Рахимбаев. – Ташкент, 1974. – 44 с.
3. Юхневский, П. И. О механизме пластификации цементных композиций / П. И. Юхневский // Строительная наука и техника. – 2010. – № 1–2. – С. 64–69.
4. Калашников, В. И. Основы пластифицирования минеральных дисперсных систем для производства строительных материалов: дис. … д-ра техн. наук: 05.23.05 / В. И. Калашников. – Воронеж, 1996. – 89 с.
5. Юсупов, Р. К. Исследование путей повышения эффективности химических добавок на основе лигносульфонатов / Р. К. Юсупов, В. Г. Карпис, В. Л. Гольдштейн: Новые разработки в области усовершенствования производства железобетонных, бетонных и других строительных конструкций на предприятиях Главмоспромстройматериалов. – М., 1985. – С. 48–56.
6. Фаликман, В. Р. Новое поколение суперпластификаторов / В. Р. Фаликман, А. Я. Вайнер, Н. Ф. Башлыков // Бетон и железобетон. – 2000. – № 5. – С. 5–7.
7. Stewart, J. J. P. Mopac: a semiempirical molecular orbital program / J. J. P. Stewart // J. Comput. ? Aided Mol. Des. – 1990. – V. 4, № 1. – P. 1–105.
8. Stewart, J. J. P. Optimization of Parameters for Semiempirical Methods V: Modification of NDDO Approximations and Application to 70 Elements / J. J. P. Stewart // J. Mol. Mod. – V. 13. – P. 1173–1213.
9. Артеменко, А. И. Органическая химия / А. И. Артеменко. – М.: Высшая школа, 2002. – 559 с.
10. Мартынович, С. И. Физико-химические предпосылки совершенствования известных и разработки новых пластифицирующих добавок для цементно-водных дисперсных композиций / С. И. Мартынович, П. И. Юхневский, Н. Л. Полейко: матер. конф. «Полимеры и цементы в строительстве», т. 2. – Тюмень, 1990. – С. 216–220.
11. Юхневский, П. И. О корреляционной связи водоредуцирующей эффективности с величиной дипольного момента химической добавки-пластификатора / П. И. Юхневский, В. М. Зеленковский, В. С. Солдатов // Технология бетонов. – 2010. – № 9–10. – С. 28, 29.
12. Добавки для бетонов. Общие технические условия: СТБ 1112-98. – Введ. 01.01.1999.